Une imprimante 3D. Un peu de cellulose bactérienne. Quelques algues. Et voici qu'un matériau vivant se crée tout seul. Enfin... presque. Les recettes pour des matériaux dits vivants, puisque fabriqués en encapsulant des cellules biologiques vivantes dans une matrice, ont fleuri ces dernières années. Récemment, des chercheurs ont rapporté une technique de bio-impression débouchant sur une matière aux propriétés remarquables.
Ces scientifiques ont enfermé des microalgues dans un produit excrété par des bactéries, vulgairement nommé « cellulose bactérienne ». Les microalgues confèrent des capacités photosynthétiques à l'étoffe obtenue. Ce qui lui permet, notamment, de se régénérer. Les auteurs de l'étude précisent qu'elle peut « survivre de manière stable pendant au moins trois jours sans nutriments », sa durée de vie pouvant être prolongée si elle est transférée vers une nouvelle source de nutriments durant cette période.
Un levain textile
Pour la première fois, ce matériau photosynthétique semble assez performant pour être déployé dans « des applications du monde réel », avance Anne Meyer, biologiste américaine et coautrice du papier. Résistant. Tenace. Flexible. Robuste. Il a tout pour plaire. Déformé d'une façon ou d'une autre, il conserve son intégrité physique. Les chercheurs lui attribuent trois applications principales : la création de feuilles artificielles, de vêtements biologiques, et de peaux photosynthétiques.
Les feuilles artificielles imitent la photosynthèse des feuilles végétales, c'est-à-dire qu'elles convertissent l'eau et le CO2 en oxygène et en énergie, grâce à la lumière du soleil. Cette innovation fait partie des solutions envisagées pour produire de l'énergie et de l'oxygène dans des endroits peu propices à la végétation... comme Mars. En parallèle, les « peaux synthétiques » serviraient pour les greffes de peau. Anne Meyer explique que « l'oxygène généré aiderait à relancer la cicatrisation de la zone endommagée, ou pourrait être capable de réaliser une cicatrisation"activée par la lumière" des plaies ».
Ce matériau pourrait révolutionner le secteur du textile. De la mode. Les vêtements créés seraient biodégradables et évolutifs. Un pantalon troué se régénererait, mais un pantalon trop petit pourrait aussi grandir. Si ce n'est qu'hypothétique à l'heure actuelle, cela enlèverait une sacrée épine dans le pied de cette industrie -- l'une des plus polluantes de la Planète. Ces matériaux « peuvent se maintenir sur des périodes de plusieurs semaines et être multipliés sur place, de sorte qu'ils ont le potentiel d'être vraiment durables et partagés partout dans le monde, aussi facilement que le levain », se prend à rêver Anne Meyer.
Ces scientifiques ont enfermé des microalgues dans un produit excrété par des bactéries, vulgairement nommé « cellulose bactérienne ». Les microalgues confèrent des capacités photosynthétiques à l'étoffe obtenue. Ce qui lui permet, notamment, de se régénérer. Les auteurs de l'étude précisent qu'elle peut « survivre de manière stable pendant au moins trois jours sans nutriments », sa durée de vie pouvant être prolongée si elle est transférée vers une nouvelle source de nutriments durant cette période.
Un levain textile
Pour la première fois, ce matériau photosynthétique semble assez performant pour être déployé dans « des applications du monde réel », avance Anne Meyer, biologiste américaine et coautrice du papier. Résistant. Tenace. Flexible. Robuste. Il a tout pour plaire. Déformé d'une façon ou d'une autre, il conserve son intégrité physique. Les chercheurs lui attribuent trois applications principales : la création de feuilles artificielles, de vêtements biologiques, et de peaux photosynthétiques.
Les feuilles artificielles imitent la photosynthèse des feuilles végétales, c'est-à-dire qu'elles convertissent l'eau et le CO2 en oxygène et en énergie, grâce à la lumière du soleil. Cette innovation fait partie des solutions envisagées pour produire de l'énergie et de l'oxygène dans des endroits peu propices à la végétation... comme Mars. En parallèle, les « peaux synthétiques » serviraient pour les greffes de peau. Anne Meyer explique que « l'oxygène généré aiderait à relancer la cicatrisation de la zone endommagée, ou pourrait être capable de réaliser une cicatrisation"activée par la lumière" des plaies ».
Ce matériau pourrait révolutionner le secteur du textile. De la mode. Les vêtements créés seraient biodégradables et évolutifs. Un pantalon troué se régénererait, mais un pantalon trop petit pourrait aussi grandir. Si ce n'est qu'hypothétique à l'heure actuelle, cela enlèverait une sacrée épine dans le pied de cette industrie -- l'une des plus polluantes de la Planète. Ces matériaux « peuvent se maintenir sur des périodes de plusieurs semaines et être multipliés sur place, de sorte qu'ils ont le potentiel d'être vraiment durables et partagés partout dans le monde, aussi facilement que le levain », se prend à rêver Anne Meyer.

source: fr.yna.co.kr

EOUL, 10 mai (Yonhap) -- La société pharmaceutique sud-coréenne Celltrion Inc. a annoncé ce lundi avoir conclu un accord avec une société publique pakistanaise en vue d'exporter le Rekirona, marquant le lancement des ventes mondiales de ce médicament à base d'anticorps contre le nouveau coronavirus (Covid-19).
En vertu de ce contrat signé avec une filiale de Pakistan Ordnance Factories, seront expédiés 100.000 flacons du Rekirona, un volume pouvant être administré à environ 30.000 personnes.
En outre, Celltrion enverra une équipe médicale afin d'offrir un programme de formation aux médecins et infirmières qui administreront ce médicament.
e Pakistan, qui compte plus de 216 millions d'habitants, fait face à de grandes difficultés pour lutter contre le Covid-19 en rapportant en moyenne environ 4.000 cas journaliers de Covid-19.
La société sud-coréenne s'attend à ce que le Regkirona aide à améliorer la situation sanitaire et à alléger la charge des personnels soignants au Pakistan.
«Nous sommes en train de discuter des exportations du Rekirona avec d'autres pays d'Europe, d'Amérique latine et l'Inde», a déclaré un responsable de l'entreprise.
En février dernier, le Rekirona a reçu une approbation conditionnelle auprès du ministère sud-coréen de la Sécurité des denrées alimentaires et des médicaments.
Le Rekirona est un anticorps monoclonal ayant une activité contre le Covid-19. Un anticorps monoclonal est un type de protéine qui a été conçu pour se fixer à une structure spécifique.
Le traitement est administré aux patients atteints du Covid-19 à risque élevé, notamment les personnes âgées de 60 ans et plus, ou souffrant de maladies cardiaques, de diabète, d'hypertension ou de maladies chroniques qui affectent le système respiratoire. Il a été administré à plus de 2.700 patients du Covid-19 en Corée du Sud.
Celltrion est en train d'analyser les données récoltées à travers des essais cliniques mondiaux de phase 3 menés sur 1.300 personnes dans 13 pays comme la Corée du Sud, les Etats-Unis, l'Espagne et la Roumanie.

 source: sciencemag.org
source: sciencemag.orgA team of prominent scientists has doubled down on its controversial hypothesis that genetic bits of the pandemic coronavirus can integrate into our chromosomes and stick around long after the infection is over. If they are right?skeptics have argued that their results are likely lab artifacts?the insertions could explain the rare finding that people can recover from COVID-19 but then test positive for SARS-CoV-2 again months later.
Stem cell biologist Rudolf Jaenisch and gene regulation specialist Richard Young of the Massachusetts Institute of Technology, who led the work, triggered a Twitter storm in December 2020, when their team first presented the idea in a preprint on bioRxiv. The researchers emphasized that viral integration did not mean people who recovered from COVID-19 remain infectious. But critics charged them with stoking unfounded fears that COVID-19 vaccines based on messenger RNA (mRNA) might somehow alter human DNA. (Janesich and Young stress that their results, both original and new, in no way imply that those vaccines integrate their sequences into our DNA.)
Researchers also presented a brace of scientific criticisms, some of which the team addresses in a paper released online today by the Proceedings of the National Academy of Sciences (PNAS). ?We now have unambiguous evidence that coronavirus sequences can integrate into the genome,? Jaenisch says.
SARS-CoV-2, the virus that causes COVID-19, has genes composed of RNA, and Jaenisch, Young, and co-authors contend that on rare occasions an enzyme in human cells may copy the viral sequences into DNA and slip them into our chromosomes. The enzyme, reverse transcriptase, is encoded by LINE-1 elements, sequences that litter 17% of the human genome and represent artifacts of ancient infections by retroviruses. In their original preprint, the researchers presented test tube evidence that when human cells spiked with extra LINE-1 elements were infected with the coronavirus, DNA versions of SARS-CoV-2's sequences nestled into the cells' chromosomes.
Many researchers who specialize in LINE-1 elements and other ?retrotransposons? thought the data were too thin to support the claim. ?If I would have had this data, I would have not submitted to any publication at that point,? says Cornell University's Cedric Feschotte, who studies endogenous retrovirus chunks in the human genome. He and others also said they expected higher quality work coming from scientists of the caliber of Jaenisch and Young. In two subsequent studies, both posted on bioRxiv, critics presented evidence that the supposed chimeras of human and viral DNA traces are routinely created by the very technique the group used to scan for them in chromosomes. As one report concluded, the human-virus sequences ?are more likely to be a methodological product, [sic] than the result of genuine reverse transcription, integration and expression.?
In their new paper, Jaenisch, Young, and colleagues acknowledge that the technique they used accidentally creates human-viral chimeras. ?I think it's a valid point,? Jaenisch says. He adds that when they first submitted the paper to a journal, they knew it needed stronger data, which they hoped to add during the review process. But the journal, like many, requires authors to immediately post all COVID-19 results to a preprint server. ?I probably should have said screw you, I won't put it on bioRxiv. It was a misjudgment,? Jaenisch says.
In the new PNAS paper, the team provides evidence that artifacts alone can't explain the detected levels of virus-human chimeric DNA. The scientists also show that portions of LINE-1 elements flank the integrated viral genetic sequence, further supporting their hypothesis. And they have collaborated with one of the original skeptics, Stephen Hughes of the National Cancer Institute, who suggested an experiment to clarify whether the integration was real or noise, based on the orientation of the integrated viral sequences relative to the human ones. The results support the original hypothesis, says Hughes, a co-author of the new paper. ?That analysis has turned out to be important,? he says.
?The integration data in cell culture is much more convincing than what was presented in the preprint, but it's still not totally clean,? says Feschotte, who now calls Jaenisch's and Young's hypothesis ?plausible.? (SARS-CoV-2, he notes, can also persist in a person for months without integrating its genes.)
The real question is whether the cell culture data have any relevance to human health or diagnostics. ?In the absence of evidence of integration in patients, the most I can take away from these data is that it is possible to detect SARS-CoV-2 RNA retroposition events in infected cell lines where L1 is overexpressed,? Feschotte says. ?The clinical or biological significance of these observations, if any, is a matter of pure speculation at this point.?
Jaenisch's and Young's team do report hints of SARS-CoV-2 integration in tissue from living and autopsied COVID-19 patients. Specifically, the researchers found high levels of a type of RNA that is only produced by integrated viral DNA as the cell reads its sequence to make proteins. But, Young acknowledges, ?We do not have direct evidence for that yet.?
Harmit Malik, a specialist in ancient viruses in the human genome at the Fred Hutchinson Cancer Research Center, says it's a ?legitimate question? to ask why people who should have cleared the virus sometimes have positive polymerase chain Reaction tests for its sequences. But he also remains unconvinced that the explanation is integrated virus. ?Under normal circumstances, there is so little reverse transcription machinery available? in human cells, Malik says.
The controversy has grown decidedly more civil since December. Both Young and Jaenisch say they received more intense criticism for their preprint than any studies in their careers, in part because some researchers worried it played into the hands of vaccine skeptics spreading false claims about the newly authorized mRNA vaccines. ?If there ever was a preprint that should be deleted, it is this one! It was irresponsible to even put it up as a preprint, considering the complete lack of relevant evidence. This is now being used by some to spread doubts about the new vaccines,? Marie-Louise Hammarskjöld, a microbiologist at the University of Virginia, posted in a comment on bioRxiv at the time.
Voir aussi: https://www.pnas.org/content/118/21/e2105968118
Stem cell biologist Rudolf Jaenisch and gene regulation specialist Richard Young of the Massachusetts Institute of Technology, who led the work, triggered a Twitter storm in December 2020, when their team first presented the idea in a preprint on bioRxiv. The researchers emphasized that viral integration did not mean people who recovered from COVID-19 remain infectious. But critics charged them with stoking unfounded fears that COVID-19 vaccines based on messenger RNA (mRNA) might somehow alter human DNA. (Janesich and Young stress that their results, both original and new, in no way imply that those vaccines integrate their sequences into our DNA.)
Researchers also presented a brace of scientific criticisms, some of which the team addresses in a paper released online today by the Proceedings of the National Academy of Sciences (PNAS). ?We now have unambiguous evidence that coronavirus sequences can integrate into the genome,? Jaenisch says.
SARS-CoV-2, the virus that causes COVID-19, has genes composed of RNA, and Jaenisch, Young, and co-authors contend that on rare occasions an enzyme in human cells may copy the viral sequences into DNA and slip them into our chromosomes. The enzyme, reverse transcriptase, is encoded by LINE-1 elements, sequences that litter 17% of the human genome and represent artifacts of ancient infections by retroviruses. In their original preprint, the researchers presented test tube evidence that when human cells spiked with extra LINE-1 elements were infected with the coronavirus, DNA versions of SARS-CoV-2's sequences nestled into the cells' chromosomes.
Many researchers who specialize in LINE-1 elements and other ?retrotransposons? thought the data were too thin to support the claim. ?If I would have had this data, I would have not submitted to any publication at that point,? says Cornell University's Cedric Feschotte, who studies endogenous retrovirus chunks in the human genome. He and others also said they expected higher quality work coming from scientists of the caliber of Jaenisch and Young. In two subsequent studies, both posted on bioRxiv, critics presented evidence that the supposed chimeras of human and viral DNA traces are routinely created by the very technique the group used to scan for them in chromosomes. As one report concluded, the human-virus sequences ?are more likely to be a methodological product, [sic] than the result of genuine reverse transcription, integration and expression.?
In their new paper, Jaenisch, Young, and colleagues acknowledge that the technique they used accidentally creates human-viral chimeras. ?I think it's a valid point,? Jaenisch says. He adds that when they first submitted the paper to a journal, they knew it needed stronger data, which they hoped to add during the review process. But the journal, like many, requires authors to immediately post all COVID-19 results to a preprint server. ?I probably should have said screw you, I won't put it on bioRxiv. It was a misjudgment,? Jaenisch says.
In the new PNAS paper, the team provides evidence that artifacts alone can't explain the detected levels of virus-human chimeric DNA. The scientists also show that portions of LINE-1 elements flank the integrated viral genetic sequence, further supporting their hypothesis. And they have collaborated with one of the original skeptics, Stephen Hughes of the National Cancer Institute, who suggested an experiment to clarify whether the integration was real or noise, based on the orientation of the integrated viral sequences relative to the human ones. The results support the original hypothesis, says Hughes, a co-author of the new paper. ?That analysis has turned out to be important,? he says.
?The integration data in cell culture is much more convincing than what was presented in the preprint, but it's still not totally clean,? says Feschotte, who now calls Jaenisch's and Young's hypothesis ?plausible.? (SARS-CoV-2, he notes, can also persist in a person for months without integrating its genes.)
The real question is whether the cell culture data have any relevance to human health or diagnostics. ?In the absence of evidence of integration in patients, the most I can take away from these data is that it is possible to detect SARS-CoV-2 RNA retroposition events in infected cell lines where L1 is overexpressed,? Feschotte says. ?The clinical or biological significance of these observations, if any, is a matter of pure speculation at this point.?
Jaenisch's and Young's team do report hints of SARS-CoV-2 integration in tissue from living and autopsied COVID-19 patients. Specifically, the researchers found high levels of a type of RNA that is only produced by integrated viral DNA as the cell reads its sequence to make proteins. But, Young acknowledges, ?We do not have direct evidence for that yet.?
Harmit Malik, a specialist in ancient viruses in the human genome at the Fred Hutchinson Cancer Research Center, says it's a ?legitimate question? to ask why people who should have cleared the virus sometimes have positive polymerase chain Reaction tests for its sequences. But he also remains unconvinced that the explanation is integrated virus. ?Under normal circumstances, there is so little reverse transcription machinery available? in human cells, Malik says.
The controversy has grown decidedly more civil since December. Both Young and Jaenisch say they received more intense criticism for their preprint than any studies in their careers, in part because some researchers worried it played into the hands of vaccine skeptics spreading false claims about the newly authorized mRNA vaccines. ?If there ever was a preprint that should be deleted, it is this one! It was irresponsible to even put it up as a preprint, considering the complete lack of relevant evidence. This is now being used by some to spread doubts about the new vaccines,? Marie-Louise Hammarskjöld, a microbiologist at the University of Virginia, posted in a comment on bioRxiv at the time.
Voir aussi: https://www.pnas.org/content/118/21/e2105968118

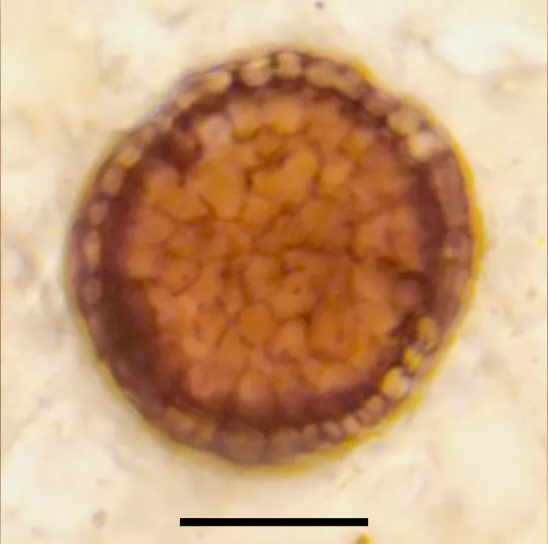 source: fredzone.org
source: fredzone.orgSelon une étude récemment parue dans Live Science, des scientifiques auraient découvert le fossile du plus vieil organisme multicellulaire. Les archéologues ont retrouvé cette relique, dont l'âge est estimé à un milliard d'années, dans ce qui était autrefois un lac des hautes terres écossaises.
Grâce à des analyses minutieuses, les chercheurs ont été en mesure de faire plusieurs découvertes concernant cet organisme baptisé Bicellum brasieri.
Les études ont également permis de réaliser une autre découverte surprenante. En effet, alors que l'on a toujours pensé que les océans étaient à l'origine de toutes les anciennes formes de vie, mettre la main sur le Bicellum brasieri nous prouve que ce ne fut pas toujours le cas.
Un fossile comme on n'en a jamais vu auparavant
Cet organisme multicellulaire fait à peine 0,03 mm de diamètre et a donc été retrouvé dans des nodules de minéraux phosphatés épais d'environ 1 cm. Durant leur expérience, Charles Wellman de l'Université de Sheffield (Angleterre) et son équipe ont coupé ces nodules avec une scie diamantée, afin d'obtenir des couches suffisamment minces pour permettre à la lumière de passer.
Les analyses au microscope ont ensuite permis de faire une incroyable découverte. Cet organisme fossilisé était composé de deux types de cellules bien distincts. Tandis que certaines d'entre elles étaient rondes et disposaient de parois fines, les autres cellules avaient une forme plutôt étirée et avaient d'épaisses parois. Ce qui indique clairement qu'il s'agit d'un organisme multicellulaire.
Selon les chercheurs, chacun des échantillons étudiés a montré les cellules de cet organisme à différentes étapes de leur évolution. Ainsi, pour les chercheurs cet organisme était bel et bien un être vivant.
Ce fossile remet une célèbre théorie en question
Selon Wellman et son équipe, le Bicellum brasieri pourrait faire partie de la famille des Holozoaires, un groupe d'anciens organismes étroitement liés aux animaux.
Pour rappel, la communauté scientifique a depuis toujours avancé que l'océan était à l'origine du développement de la vie sur notre planète. Cela est en partie dû au fait que les chercheurs ont retrouvé la majorité des fossiles des premiers êtres vivants dans les fonds marins.
Mais vu que le fossile de Bicellum brasieri avait apparemment vécu dans ce qui était autrefois un lac, les scientifiques en concluent que d'autres milieux avaient aussi leurs rôles à jouer dans l'émergence de la vie sur Terre.
Source d'information: https://www.livescience.com/billion-year-old-fossil-animal-evolution.html
Grâce à des analyses minutieuses, les chercheurs ont été en mesure de faire plusieurs découvertes concernant cet organisme baptisé Bicellum brasieri.
Les études ont également permis de réaliser une autre découverte surprenante. En effet, alors que l'on a toujours pensé que les océans étaient à l'origine de toutes les anciennes formes de vie, mettre la main sur le Bicellum brasieri nous prouve que ce ne fut pas toujours le cas.
Un fossile comme on n'en a jamais vu auparavant
Cet organisme multicellulaire fait à peine 0,03 mm de diamètre et a donc été retrouvé dans des nodules de minéraux phosphatés épais d'environ 1 cm. Durant leur expérience, Charles Wellman de l'Université de Sheffield (Angleterre) et son équipe ont coupé ces nodules avec une scie diamantée, afin d'obtenir des couches suffisamment minces pour permettre à la lumière de passer.
Les analyses au microscope ont ensuite permis de faire une incroyable découverte. Cet organisme fossilisé était composé de deux types de cellules bien distincts. Tandis que certaines d'entre elles étaient rondes et disposaient de parois fines, les autres cellules avaient une forme plutôt étirée et avaient d'épaisses parois. Ce qui indique clairement qu'il s'agit d'un organisme multicellulaire.
Selon les chercheurs, chacun des échantillons étudiés a montré les cellules de cet organisme à différentes étapes de leur évolution. Ainsi, pour les chercheurs cet organisme était bel et bien un être vivant.
Ce fossile remet une célèbre théorie en question
Selon Wellman et son équipe, le Bicellum brasieri pourrait faire partie de la famille des Holozoaires, un groupe d'anciens organismes étroitement liés aux animaux.
Pour rappel, la communauté scientifique a depuis toujours avancé que l'océan était à l'origine du développement de la vie sur notre planète. Cela est en partie dû au fait que les chercheurs ont retrouvé la majorité des fossiles des premiers êtres vivants dans les fonds marins.
Mais vu que le fossile de Bicellum brasieri avait apparemment vécu dans ce qui était autrefois un lac, les scientifiques en concluent que d'autres milieux avaient aussi leurs rôles à jouer dans l'émergence de la vie sur Terre.
Source d'information: https://www.livescience.com/billion-year-old-fossil-animal-evolution.html

source: Youtube: REINFO COVID TV
[vidéo supprimée sur YouTube]
Astra Zeneca
Vecteur viraux non - réplicatif = Utilisation d'un virus modifié pour faire produire la protéine spike
par les cellules de la personne vaccinée.
Vecteurs viraux choisis sont adenovirus. On les a modifié génétiquement.
Deux types: gènes essentielles à la réplication du virus ont été supprimés.
On a inséré des gênes d'intérêt = production par les cellules vacinées de la protéine spike.
= Production d'anticorps anti-spike par l'organisme vacinné.
Vecteurs viraux sont produits à partir de cellules humaines génétiquement modifié. (embryon, rein)
Risques: Processus de replication par recombinaison.
Purification jamais complète de cellules humaines.
Un embryon avorté a été récupéré, puis a été modifié, puis cultivé.
Mécanisme:
Adenovirus rentre dans la cellule, il va relarguer son adn à l'intérieur de la cellule de la personne vacciné,
puis, transmis et produit par la cellule du vacciné et produit des anticorps.
Composition
Adenovirus de chimpanzé génétiquement modifié pour être non réplicatif.
[vidéo supprimée sur YouTube]
Pfizer
Principe actif
ARN messagé a été modifié de deux manières:
les uridines ont été transformées en methyl-pseudo-uridine
Deux mutations des acides aminés.
C'est une suite de nucléotides. Chaque triplé code un acide aminé.
L'arn messagé ne code pas pour la protéine spike naturelle.
Excipients
deux de ces excipients n'ont pas été autorisés en europe.
Impureté
arn tronqués = petits morceaux de cette arn.
Risques: On ne connait pas la quantité de arn tronqué. On ne sait pas si sont traduits en protéine, et si oui, lesquelles.
On ne connaît pas le principe actif exact. Risque de maladies auto-immune.
Résidus d'ADN
limite basses, mais non défini... Peut s'intégrer dans le génome.
[vidéo supprimée sur YouTube]
Astra Zeneca
Vecteur viraux non - réplicatif = Utilisation d'un virus modifié pour faire produire la protéine spike
par les cellules de la personne vaccinée.
Vecteurs viraux choisis sont adenovirus. On les a modifié génétiquement.
Deux types: gènes essentielles à la réplication du virus ont été supprimés.
On a inséré des gênes d'intérêt = production par les cellules vacinées de la protéine spike.
= Production d'anticorps anti-spike par l'organisme vacinné.
Vecteurs viraux sont produits à partir de cellules humaines génétiquement modifié. (embryon, rein)
Risques: Processus de replication par recombinaison.
Purification jamais complète de cellules humaines.
Un embryon avorté a été récupéré, puis a été modifié, puis cultivé.
Mécanisme:
Adenovirus rentre dans la cellule, il va relarguer son adn à l'intérieur de la cellule de la personne vacciné,
puis, transmis et produit par la cellule du vacciné et produit des anticorps.
Composition
Adenovirus de chimpanzé génétiquement modifié pour être non réplicatif.
[vidéo supprimée sur YouTube]
Pfizer
Principe actif
ARN messagé a été modifié de deux manières:
les uridines ont été transformées en methyl-pseudo-uridine
Deux mutations des acides aminés.
C'est une suite de nucléotides. Chaque triplé code un acide aminé.
L'arn messagé ne code pas pour la protéine spike naturelle.
Excipients
deux de ces excipients n'ont pas été autorisés en europe.
Impureté
arn tronqués = petits morceaux de cette arn.
Risques: On ne connait pas la quantité de arn tronqué. On ne sait pas si sont traduits en protéine, et si oui, lesquelles.
On ne connaît pas le principe actif exact. Risque de maladies auto-immune.
Résidus d'ADN
limite basses, mais non défini... Peut s'intégrer dans le génome.
[vidéo supprimée sur YouTube]

source: fr.futuroprossimo.it
Deepdub, La start-up israélienne de doublage avec l'intelligence artificielle a commencé à devenir sérieuse. La société a conclu un accord pour traduire le film «Every Time I Die», actuellement diffusé sur UK Netflix pour les Amériques.
Deepdub utilisera sa technologie de synthèse vocale AI pour doubler le film en espagnol d'Amérique latine et en portugais brésilien. Les versions résultantes contiendront des voix qui sonnent exactement comme celles des acteurs originaux.
Une révolution dans le doublage
«Nous capturerons avec précision le style vocal et les attributs vocaux des acteurs originaux, et ils seront adaptés à la langue cible», explique Oz Krakowski, PDG de Deepdub. "Dans ce cas, le doublage en espagnol latino-américain et en portugais brésilien nécessite des adaptations différentes."
Quelques informations sur Deepdub, la technologie qui peut transformer le monde du doublage (et même des films) grâce à l'intelligence artificielle:
Deepdub il est sorti tranquillement en décembre offrant des doublages basés sur l'IA pour des publicités et d'autres projets dans six langues cibles.
La copie d'un film complet prend plus de temps. Pour Krakowski, le processus pourrait prendre jusqu'à huit semaines. «Nous avons intégré des procédures de contrôle de qualité manuelles et automatiques avancées», dit-il. «Le processus comprend un directeur de doublage et un expert linguistique qui examine le résultat final. Leurs commentaires sont réinjectés dans la machine pour améliorer les résultats et affiner le processus automatique dans les projets futurs ».
Inutile de dire que l'IA est beaucoup moins chère que le doublage manuel. Des risques pour la profession de doubleur? Oui et non. Des opportunités pour les producteurs indépendants d'atteindre un public plus large pour leurs ?uvres? Oui bien sûr.
Et d'un autre côté, MiLa Media elle-même, qui a produit «Every Time I Die», a profité de cette possibilité. Ohad Ashkenazi, le PDG de MiLa Media, a l'intention de se tourner vers Netflix pour distribuer également des versions avec doublage dans d'autres langues, mais traite également directement avec plusieurs grands distributeurs sur le marché latino-américain.
Ce pourrait être la première fois pour toute l'industrie. Et même si Netflix ne diffuse pas plus tard les versions doublées, ce n'est qu'une question de temps avant qu'un film ou une émission de télévision sur ce service de streaming ne reçoive un doublage AI. Dans quelques années, cette technologie pourrait bouleverser les films tels que nous les connaissons.
Les acteurs étrangers les plus connus parleront dans notre langue avec le même timbre de voix qu'ils ont dans leur langue. Probablement un jour, le mouvement des lèvres changera également (la technologie est déjà à l'étude).
Voir: https://deepdub.ai/
Deepdub utilisera sa technologie de synthèse vocale AI pour doubler le film en espagnol d'Amérique latine et en portugais brésilien. Les versions résultantes contiendront des voix qui sonnent exactement comme celles des acteurs originaux.
Une révolution dans le doublage
«Nous capturerons avec précision le style vocal et les attributs vocaux des acteurs originaux, et ils seront adaptés à la langue cible», explique Oz Krakowski, PDG de Deepdub. "Dans ce cas, le doublage en espagnol latino-américain et en portugais brésilien nécessite des adaptations différentes."
Quelques informations sur Deepdub, la technologie qui peut transformer le monde du doublage (et même des films) grâce à l'intelligence artificielle:
Deepdub il est sorti tranquillement en décembre offrant des doublages basés sur l'IA pour des publicités et d'autres projets dans six langues cibles.
La copie d'un film complet prend plus de temps. Pour Krakowski, le processus pourrait prendre jusqu'à huit semaines. «Nous avons intégré des procédures de contrôle de qualité manuelles et automatiques avancées», dit-il. «Le processus comprend un directeur de doublage et un expert linguistique qui examine le résultat final. Leurs commentaires sont réinjectés dans la machine pour améliorer les résultats et affiner le processus automatique dans les projets futurs ».
Inutile de dire que l'IA est beaucoup moins chère que le doublage manuel. Des risques pour la profession de doubleur? Oui et non. Des opportunités pour les producteurs indépendants d'atteindre un public plus large pour leurs ?uvres? Oui bien sûr.
Et d'un autre côté, MiLa Media elle-même, qui a produit «Every Time I Die», a profité de cette possibilité. Ohad Ashkenazi, le PDG de MiLa Media, a l'intention de se tourner vers Netflix pour distribuer également des versions avec doublage dans d'autres langues, mais traite également directement avec plusieurs grands distributeurs sur le marché latino-américain.
Ce pourrait être la première fois pour toute l'industrie. Et même si Netflix ne diffuse pas plus tard les versions doublées, ce n'est qu'une question de temps avant qu'un film ou une émission de télévision sur ce service de streaming ne reçoive un doublage AI. Dans quelques années, cette technologie pourrait bouleverser les films tels que nous les connaissons.
Les acteurs étrangers les plus connus parleront dans notre langue avec le même timbre de voix qu'ils ont dans leur langue. Probablement un jour, le mouvement des lèvres changera également (la technologie est déjà à l'étude).
Voir: https://deepdub.ai/

source: siecledigital.fr
Des scientifiques du Wyss Institute for Biologically Inspired Engineering d'Harvard ont créé un outil d'édition génomique, soit une technique de manipulation du génome [ensemble du matériel génétique d'une espèce codé dans son ADN] visant à la modification du matériel génétique. L'avancée baptisée Retron Library Recombineering (RLR) vient répondre à certaines problématiques de CRISPR, la technique d'édition génomique actuellement la plus reconnue et qui a fait plusieurs fois la une, notamment à la suite de son utilisation pour modifier l'ADN d'embryons humains.
La RLR s'appuie sur les retrons, soit des séquences génétiques présentes dans certaines bactéries qui produisent un brin d'ADN unique. Vulgairement, la RLR consiste à introduire dans une cellule une mutation sous la forme de brin d'ADN pendant qu'elle est dans la phase de réplique de son génome. Par la suite, les cellules s?urs créées répliquent naturellement la mutation. « La RLR est un outil d'édition génétique plus simple et plus flexible qui peut être utilisé pour des expériences hautement multiplexées », soutient Max Schubert, l'un des coauteurs de l'étude.
Les retrons permettent la production et la sélection rapides de millions de variations d'ADN traçables et de leurs conséquences sur les bactéries en simultané. Crédit : Max Schubert / Institut Wyss de l'université de Harvard
La technique actuelle, CRISPR, permet de modifier les séquences d'ADN grâce à des « ciseaux génétiques » : l'enzyme Cas9. Simplement, CRISPR permet d'ajouter, supprimer ou modifier le patrimoine génétique de n'importe quelle cellule. La technique s'est montrée prometteuse, notamment pour la recherche contre le cancer. Néanmoins, le matériel requis pour CRISPR est difficile à installer en grande quantité, ce qui complexifie la recherche. Par ailleurs, l'enzyme Cas9 sur lequel CRISPR s'appuie pour couper les brins d'ADN n'est pas toujours précis et peut couper des éléments non-ciblés.
Contrairement à CRISPR, avec la RLR, l'ADN n'est pas cassé, ce qui supprime « la toxicité souvent observée avec CRISPR ». Aussi, les retrons font office de « code-barre » et permettent une identification. Ainsi, les chercheurs peuvent faire de l'édition génomique sur plusieurs cibles dans lesquelles ils veulent insérer des mutations. La RLR pourra être utilisée conjointement avec CRISPR ou servir de remplacement quand le découpage est trop délicat.
La RLR peut « conduire à des innovations nouvelles, passionnantes et inattendues »
« Nous avons pensé que les retrons devraient nous donner la capacité de produire de l'ADN simple brin à l'intérieur des cellules que nous voulions modifier, plutôt que d'essayer de les forcer à entrer dans la cellule de l'extérieur, et sans endommager l'ADN natif, deux qualités très convaincantes », explique Daniel Goodman, ancien doctorant de l'Institut Wyss.
Le groupe de recherche d'Harvard a testé la RLR sur des bactéries E. coli et ont observé que 90% de la population incorporait la séquence après quelques modifications. Pendant leurs expériences, les scientifiques ont pu trouver des mutations de résistance aux antibiotiques au sein de la bactérie E. coli en séquençant le « code-barre » des retrons - au lieu de séquencer les mutants - rendant ainsi la procédure nettement plus rapide.
« La RLR nous a permis de faire quelque chose d'impossible avec CRISPR : nous avons découpé aléatoirement un génome bactérien, nous avons transformé ces fragments génétiques en ADN simple brin in situ, et nous les avons utilisés pour cribler des millions de séquences simultanément », détaille Max Schubert.
Malgré ses avancées encourageantes, il reste du chemin à parcourir avant que la RLR soit utilisée à grande échelle, notamment sur l'amélioration et la standardisation de son taux d'édition. Néanmoins, l'équipe du Wyss Institute estime qu'elle peut « conduire à des innovations nouvelles, passionnantes et inattendues ».
Voir aussi: https://fr.futuroprossimo.it/2021/05/harvard-crea-rlr-editing-genetico-che-puo-superare-crispr-con-i-retroni/
La RLR s'appuie sur les retrons, soit des séquences génétiques présentes dans certaines bactéries qui produisent un brin d'ADN unique. Vulgairement, la RLR consiste à introduire dans une cellule une mutation sous la forme de brin d'ADN pendant qu'elle est dans la phase de réplique de son génome. Par la suite, les cellules s?urs créées répliquent naturellement la mutation. « La RLR est un outil d'édition génétique plus simple et plus flexible qui peut être utilisé pour des expériences hautement multiplexées », soutient Max Schubert, l'un des coauteurs de l'étude.
Les retrons permettent la production et la sélection rapides de millions de variations d'ADN traçables et de leurs conséquences sur les bactéries en simultané. Crédit : Max Schubert / Institut Wyss de l'université de Harvard
La technique actuelle, CRISPR, permet de modifier les séquences d'ADN grâce à des « ciseaux génétiques » : l'enzyme Cas9. Simplement, CRISPR permet d'ajouter, supprimer ou modifier le patrimoine génétique de n'importe quelle cellule. La technique s'est montrée prometteuse, notamment pour la recherche contre le cancer. Néanmoins, le matériel requis pour CRISPR est difficile à installer en grande quantité, ce qui complexifie la recherche. Par ailleurs, l'enzyme Cas9 sur lequel CRISPR s'appuie pour couper les brins d'ADN n'est pas toujours précis et peut couper des éléments non-ciblés.
Contrairement à CRISPR, avec la RLR, l'ADN n'est pas cassé, ce qui supprime « la toxicité souvent observée avec CRISPR ». Aussi, les retrons font office de « code-barre » et permettent une identification. Ainsi, les chercheurs peuvent faire de l'édition génomique sur plusieurs cibles dans lesquelles ils veulent insérer des mutations. La RLR pourra être utilisée conjointement avec CRISPR ou servir de remplacement quand le découpage est trop délicat.
La RLR peut « conduire à des innovations nouvelles, passionnantes et inattendues »
« Nous avons pensé que les retrons devraient nous donner la capacité de produire de l'ADN simple brin à l'intérieur des cellules que nous voulions modifier, plutôt que d'essayer de les forcer à entrer dans la cellule de l'extérieur, et sans endommager l'ADN natif, deux qualités très convaincantes », explique Daniel Goodman, ancien doctorant de l'Institut Wyss.
Le groupe de recherche d'Harvard a testé la RLR sur des bactéries E. coli et ont observé que 90% de la population incorporait la séquence après quelques modifications. Pendant leurs expériences, les scientifiques ont pu trouver des mutations de résistance aux antibiotiques au sein de la bactérie E. coli en séquençant le « code-barre » des retrons - au lieu de séquencer les mutants - rendant ainsi la procédure nettement plus rapide.
« La RLR nous a permis de faire quelque chose d'impossible avec CRISPR : nous avons découpé aléatoirement un génome bactérien, nous avons transformé ces fragments génétiques en ADN simple brin in situ, et nous les avons utilisés pour cribler des millions de séquences simultanément », détaille Max Schubert.
Malgré ses avancées encourageantes, il reste du chemin à parcourir avant que la RLR soit utilisée à grande échelle, notamment sur l'amélioration et la standardisation de son taux d'édition. Néanmoins, l'équipe du Wyss Institute estime qu'elle peut « conduire à des innovations nouvelles, passionnantes et inattendues ».
Voir aussi: https://fr.futuroprossimo.it/2021/05/harvard-crea-rlr-editing-genetico-che-puo-superare-crispr-con-i-retroni/

 source: trustmyscience.com
source: trustmyscience.comIl y a quelques mois, des variantes du coronavirus SARS-CoV-2 émergeaient et inquiétaient la communauté scientifique, notamment parce qu'elles présentaient une contagiosité supérieure potentielle. Les variantes sud-africaine (B1351) et brésilienne (P1) se sont rapidement répandues et ont poussé les laboratoires pharmaceutiques à mettre à jour leurs vaccins anti-COVID. Récemment, l'entreprise Moderna a annoncé que son vaccin mis à jour avait correctement neutralisé les deux variantes au cours d'un premier essai de très petite envergure.
Le premier vaccin « modifié » contre les variantes inquiétantes du coronavirus SARS-CoV-2 qui ont émergé en Afrique du Sud et au Brésil les a neutralisés avec succès lors d'essais en laboratoire, a déclaré la société américaine Moderna. Les résultats de ce petit essai suggèrent que les rappels contre les variantes seront faisables et pourraient être déployés cette année pour contrer la menace des variantes apparues dans le monde entier et dont on craint dans certains cas d'être plus transmissibles ou partiellement résistantes aux vaccins.
Les grandes entreprises se sont battues pour produire des versions adaptées de leurs vaccins anti-COVID. Pfizer, qui possède un vaccin à ARNm similaire à celui de Moderna et Oxford/AstraZeneca, sont également en train de développer des vaccins modifiés contre la variante sud-africaine, B1351, et la variante brésilienne, P1, qui semblent être les principales menaces actuelles.
Un nouveau vaccin prometteur contre les variantes B1351 et P1
Les chercheurs de Moderna ont été les premiers à annoncer leurs résultats mercredi soir. Ils semblent très positifs, même si seules les informations de base issues d'une analyse initiale des résultats sont disponibles à ce jour. La société américaine a testé à la fois un rappel de son vaccin anti-COVID standard et une version peaufinée du vaccin chez des personnes qui avaient déjà reçu la double dose complète. Vingt adultes ont été recrutés pour chaque bras de l'essai, soit 40 au total.
Deux semaines après l'administration du nouveau vaccin, Moderna indique que le rappel et le vaccin modifié ont augmenté les anticorps dans le sang qui peuvent neutraliser les deux variantes préoccupantes. Mais le vaccin modifié ? appelé ARNm-1273.351 et conçu spécifiquement pour lutter contre les variantes sud-africaines et brésiliennes, qui ont des mutations similaires à la protéine de pointe ? a produit des niveaux plus élevés d'anticorps neutralisants que le rappel standard, l'ARNm-1273.
Moderna mène également un essai dans lequel les sujets reçoivent un mélange du rappel et du vaccin spécifiquement conçu contre la variante. Le laboratoire a soumis les premiers résultats sous forme d'article au serveur de préimpression bioRxiv ; ils ne sont donc pas encore disponibles en ligne. Une fois l'essai combiné terminé, il produira un article qui sera publié avec un examen par les pairs.
Adapter rapidement les vaccins aux nouvelles variantes
« Alors que nous cherchons à vaincre la pandémie en cours, nous restons déterminés à être proactifs à mesure que le virus évolue. Nous sommes encouragés par ces nouvelles données, qui renforcent notre confiance dans le fait que notre stratégie de booster doit être protectrice contre ces nouvelles variantes détectées », déclare Stéphane Bancel, PDG de Moderna.
« Notre plate-forme d'ARNm permet de concevoir rapidement des vaccins candidats qui incorporent des mutations virales clés, permettant potentiellement un développement plus rapide de futurs vaccins alternatifs assortis de variantes en cas de besoin? Nous continuerons à faire autant de mises à jour de notre vaccin Covid-19 que nécessaire pour contrôler la pandémie ».
Les nouveaux vaccins n'ont pas été testés sur le terrain ; ce sont des échantillons de sang de candidats analysés en laboratoire. Mais les autorités réglementaires ont déclaré qu'elles n'auraient pas besoin de passer par les essais rigoureux à grande échelle qui étaient nécessaires pour que les vaccins d'origine obtiennent une approbation d'urgence. La société a déclaré que les vaccins avaient peu d'effets secondaires et que ceux signalés étaient bénins. Outre la douleur au site d'injection, les effets secondaires les plus fréquemment rapportés étaient la fatigue, les maux de tête, les douleurs musculaires et les douleurs articulaires.
Voir aussi: https://www.nature.com/articles/d41586-021-01222-5
ET: https://www.futura-sciences.com/sante/actualites/coronavirus-anticorps-lama-pourraient-bien-etre-efficaces-variants-sars-cov-2-80857/
ET: https://www.futura-sciences.com/sante/actualites/coronavirus-pfizer-teste-pilule-covid-19-87079/#xtor%3DRSS-8
ET: https://www.mypharma-editions.com/celltrion-son-traitement-par-anticorps-monoclonal-anti-covid-19-demontre-un-effet-neutralisant-contre-le-variant-sud-africain
ET: https://www.latribune.fr/entreprises-finance/industrie/chimie-pharmacie/avec-la-biotech-spikimm-et-l-institut-pasteur-bientot-un-anticorps-francais-contre-le-covid-884051.html
On parle aussi du développement d'une immunité au COVID 19 chez les individus: https://www.pourlascience.fr/sd/immunologie/covid-19-le-systeme-immunitaire-evolue-pour-contrer-les-variants-21727.php?utm_term=Autofeed&utm_medium=Social&utm_source=Facebook&fbclid=IwAR2fv3FKcspFrAdop55HdivtpkZqofqtQS0k9lGO1NwC0fraoDiA_xLWvfE#Echobox=1620427189
https://www.caducee.net/actualite-medicale/15409/traitement-anti-covid-xav-19-fin-des-inclusions-dans-l-essai-clinique-de-phase-2b-polycor.html
Le premier vaccin « modifié » contre les variantes inquiétantes du coronavirus SARS-CoV-2 qui ont émergé en Afrique du Sud et au Brésil les a neutralisés avec succès lors d'essais en laboratoire, a déclaré la société américaine Moderna. Les résultats de ce petit essai suggèrent que les rappels contre les variantes seront faisables et pourraient être déployés cette année pour contrer la menace des variantes apparues dans le monde entier et dont on craint dans certains cas d'être plus transmissibles ou partiellement résistantes aux vaccins.
Les grandes entreprises se sont battues pour produire des versions adaptées de leurs vaccins anti-COVID. Pfizer, qui possède un vaccin à ARNm similaire à celui de Moderna et Oxford/AstraZeneca, sont également en train de développer des vaccins modifiés contre la variante sud-africaine, B1351, et la variante brésilienne, P1, qui semblent être les principales menaces actuelles.
Un nouveau vaccin prometteur contre les variantes B1351 et P1
Les chercheurs de Moderna ont été les premiers à annoncer leurs résultats mercredi soir. Ils semblent très positifs, même si seules les informations de base issues d'une analyse initiale des résultats sont disponibles à ce jour. La société américaine a testé à la fois un rappel de son vaccin anti-COVID standard et une version peaufinée du vaccin chez des personnes qui avaient déjà reçu la double dose complète. Vingt adultes ont été recrutés pour chaque bras de l'essai, soit 40 au total.
Deux semaines après l'administration du nouveau vaccin, Moderna indique que le rappel et le vaccin modifié ont augmenté les anticorps dans le sang qui peuvent neutraliser les deux variantes préoccupantes. Mais le vaccin modifié ? appelé ARNm-1273.351 et conçu spécifiquement pour lutter contre les variantes sud-africaines et brésiliennes, qui ont des mutations similaires à la protéine de pointe ? a produit des niveaux plus élevés d'anticorps neutralisants que le rappel standard, l'ARNm-1273.
Moderna mène également un essai dans lequel les sujets reçoivent un mélange du rappel et du vaccin spécifiquement conçu contre la variante. Le laboratoire a soumis les premiers résultats sous forme d'article au serveur de préimpression bioRxiv ; ils ne sont donc pas encore disponibles en ligne. Une fois l'essai combiné terminé, il produira un article qui sera publié avec un examen par les pairs.
Adapter rapidement les vaccins aux nouvelles variantes
« Alors que nous cherchons à vaincre la pandémie en cours, nous restons déterminés à être proactifs à mesure que le virus évolue. Nous sommes encouragés par ces nouvelles données, qui renforcent notre confiance dans le fait que notre stratégie de booster doit être protectrice contre ces nouvelles variantes détectées », déclare Stéphane Bancel, PDG de Moderna.
« Notre plate-forme d'ARNm permet de concevoir rapidement des vaccins candidats qui incorporent des mutations virales clés, permettant potentiellement un développement plus rapide de futurs vaccins alternatifs assortis de variantes en cas de besoin? Nous continuerons à faire autant de mises à jour de notre vaccin Covid-19 que nécessaire pour contrôler la pandémie ».
Les nouveaux vaccins n'ont pas été testés sur le terrain ; ce sont des échantillons de sang de candidats analysés en laboratoire. Mais les autorités réglementaires ont déclaré qu'elles n'auraient pas besoin de passer par les essais rigoureux à grande échelle qui étaient nécessaires pour que les vaccins d'origine obtiennent une approbation d'urgence. La société a déclaré que les vaccins avaient peu d'effets secondaires et que ceux signalés étaient bénins. Outre la douleur au site d'injection, les effets secondaires les plus fréquemment rapportés étaient la fatigue, les maux de tête, les douleurs musculaires et les douleurs articulaires.
Voir aussi: https://www.nature.com/articles/d41586-021-01222-5
ET: https://www.futura-sciences.com/sante/actualites/coronavirus-anticorps-lama-pourraient-bien-etre-efficaces-variants-sars-cov-2-80857/
ET: https://www.futura-sciences.com/sante/actualites/coronavirus-pfizer-teste-pilule-covid-19-87079/#xtor%3DRSS-8
ET: https://www.mypharma-editions.com/celltrion-son-traitement-par-anticorps-monoclonal-anti-covid-19-demontre-un-effet-neutralisant-contre-le-variant-sud-africain
ET: https://www.latribune.fr/entreprises-finance/industrie/chimie-pharmacie/avec-la-biotech-spikimm-et-l-institut-pasteur-bientot-un-anticorps-francais-contre-le-covid-884051.html
On parle aussi du développement d'une immunité au COVID 19 chez les individus: https://www.pourlascience.fr/sd/immunologie/covid-19-le-systeme-immunitaire-evolue-pour-contrer-les-variants-21727.php?utm_term=Autofeed&utm_medium=Social&utm_source=Facebook&fbclid=IwAR2fv3FKcspFrAdop55HdivtpkZqofqtQS0k9lGO1NwC0fraoDiA_xLWvfE#Echobox=1620427189
https://www.caducee.net/actualite-medicale/15409/traitement-anti-covid-xav-19-fin-des-inclusions-dans-l-essai-clinique-de-phase-2b-polycor.html

 source: demotivateur.fr
source: demotivateur.frEn Sibérie, une équipe de scientifiques russes a trouvé une plante vieille de 32 000 ans. En utilisant la technologie du clonage et le tissu placentaire des graines, les chercheurs ont réussi à la faire revivre.
En Arctique, le pergélisol fond peu à peu à cause du réchauffement climatique. Le pergélisol, aussi appelé permafrost, est une couche de glace qui se forme lorsque la température ne dépasse pas 0 degré pendant plusieurs années. En Sibérie, cette glace n'avait pas fondu depuis la préhistoire et renferme de nombreux secrets.
Pendant des années, des éléments ont été coincés dans la glace, qui a permis de les conserver en parfait état. Ainsi, des scientifiques ont pu retrouver des animaux comme des mammouths gelés, des plantes ou encore de la nourriture. La fonte du pergélisol, bien qu'elle soit une conséquence négative du réchauffement climatique, permet aux chercheurs de faire de nombreuses découvertes biologiques.
Une plante vieille de 32 000 ans revient à la vie
En 2012, une équipe de chercheurs russes a trouvé une plante gelée dans la place, appelée la Silene stenophylla, en Sibérie. Cette fleur était vieille de 32 000 ans et aurait été enterrée par un écureuil à plus de 38 mètres de profondeur.
« Elle était probablement sèche lorsqu'elle a été enterrée et quelque chose a dû se produire pour qu'elle se soit retrouvée aussi profondément dans la terre », a déclaré Margit Laimer, phytobiologiste.
Devant cette trouvaille, les chercheurs ont voulu faire revivre la plante en utilisant les gousses de la fleur. Ils ont commencé par essayer d'utiliser des graines mûres situées dans les cosses des fruits, sans succès.
Finalement, les scientifiques ont récolté du tissu encore viable sur les graines congelées, l'ont cloné, et ont pu faire vivre 36 nouvelles plantes. Un an plus tard, ces dernières ont fleuri avec succès. Quelques petites différences avec la plante d'origine ont été observées puisque les nouvelles avaient des pétales plus espacés.
Cette découverte pourrait être la clé pour apprendre d'autres secrets sur le pergélisol.
En Arctique, le pergélisol fond peu à peu à cause du réchauffement climatique. Le pergélisol, aussi appelé permafrost, est une couche de glace qui se forme lorsque la température ne dépasse pas 0 degré pendant plusieurs années. En Sibérie, cette glace n'avait pas fondu depuis la préhistoire et renferme de nombreux secrets.
Pendant des années, des éléments ont été coincés dans la glace, qui a permis de les conserver en parfait état. Ainsi, des scientifiques ont pu retrouver des animaux comme des mammouths gelés, des plantes ou encore de la nourriture. La fonte du pergélisol, bien qu'elle soit une conséquence négative du réchauffement climatique, permet aux chercheurs de faire de nombreuses découvertes biologiques.
Une plante vieille de 32 000 ans revient à la vie
En 2012, une équipe de chercheurs russes a trouvé une plante gelée dans la place, appelée la Silene stenophylla, en Sibérie. Cette fleur était vieille de 32 000 ans et aurait été enterrée par un écureuil à plus de 38 mètres de profondeur.
« Elle était probablement sèche lorsqu'elle a été enterrée et quelque chose a dû se produire pour qu'elle se soit retrouvée aussi profondément dans la terre », a déclaré Margit Laimer, phytobiologiste.
Devant cette trouvaille, les chercheurs ont voulu faire revivre la plante en utilisant les gousses de la fleur. Ils ont commencé par essayer d'utiliser des graines mûres situées dans les cosses des fruits, sans succès.
Finalement, les scientifiques ont récolté du tissu encore viable sur les graines congelées, l'ont cloné, et ont pu faire vivre 36 nouvelles plantes. Un an plus tard, ces dernières ont fleuri avec succès. Quelques petites différences avec la plante d'origine ont été observées puisque les nouvelles avaient des pétales plus espacés.
Cette découverte pourrait être la clé pour apprendre d'autres secrets sur le pergélisol.

 source: sciencesetavenir.fr
source: sciencesetavenir.frL'analyse par satellite de la biomasse de la forêt brésilienne montre que la déforestation et les dégradations du couvert émettent désormais plus de CO2 que ne peuvent en stocker les arbres. 60% de l'Amazonie n'est donc plus un puits de carbone.
Voir aussi: https://etatdurgence.ch/climat/les-puits-de-carbone-ou-de-co2/ (Pour la Suisse notamment)
https://etatdurgence.ch/wp-content/uploads/puitsdecarbone.mp3?_=1
Voir aussi: https://etatdurgence.ch/climat/les-puits-de-carbone-ou-de-co2/ (Pour la Suisse notamment)
https://etatdurgence.ch/wp-content/uploads/puitsdecarbone.mp3?_=1







 16.09.2023 - 06h34
16.09.2023 - 06h34