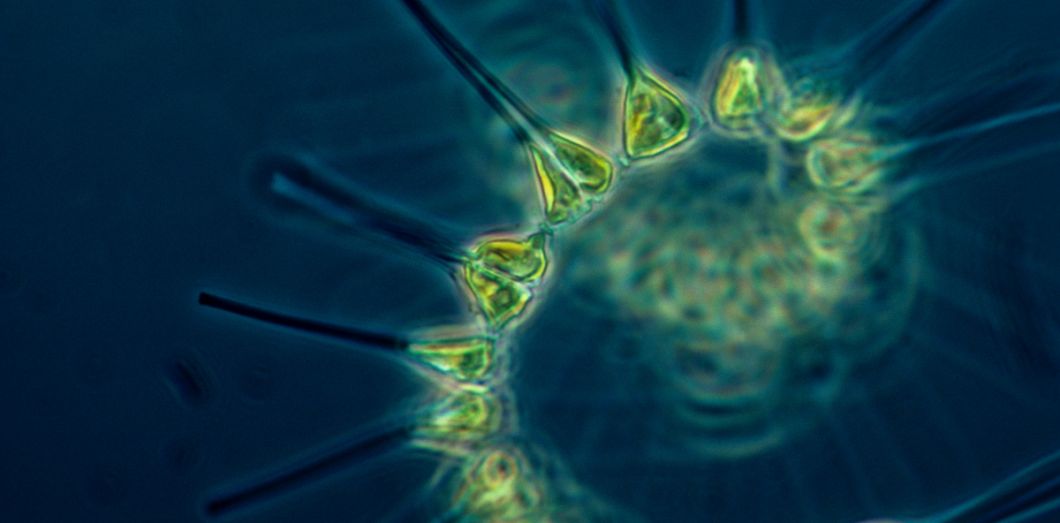
Une imprimante 3D. Un peu de cellulose bactérienne. Quelques algues. Et voici qu'un matériau vivant se crée tout seul. Enfin... presque. Les recettes pour des matériaux dits vivants, puisque fabriqués en encapsulant des cellules biologiques vivantes dans une matrice, ont fleuri ces dernières années. Récemment, des chercheurs ont rapporté une technique de bio-impression débouchant sur une matière aux propriétés remarquables.
Ces scientifiques ont enfermé des microalgues dans un produit excrété par des bactéries, vulgairement nommé « cellulose bactérienne ». Les microalgues confèrent des capacités photosynthétiques à l'étoffe obtenue. Ce qui lui permet, notamment, de se régénérer. Les auteurs de l'étude précisent qu'elle peut « survivre de manière stable pendant au moins trois jours sans nutriments », sa durée de vie pouvant être prolongée si elle est transférée vers une nouvelle source de nutriments durant cette période.
Un levain textile
Pour la première fois, ce matériau photosynthétique semble assez performant pour être déployé dans « des applications du monde réel », avance Anne Meyer, biologiste américaine et coautrice du papier. Résistant. Tenace. Flexible. Robuste. Il a tout pour plaire. Déformé d'une façon ou d'une autre, il conserve son intégrité physique. Les chercheurs lui attribuent trois applications principales : la création de feuilles artificielles, de vêtements biologiques, et de peaux photosynthétiques.
Les feuilles artificielles imitent la photosynthèse des feuilles végétales, c'est-à-dire qu'elles convertissent l'eau et le CO2 en oxygène et en énergie, grâce à la lumière du soleil. Cette innovation fait partie des solutions envisagées pour produire de l'énergie et de l'oxygène dans des endroits peu propices à la végétation... comme Mars. En parallèle, les « peaux synthétiques » serviraient pour les greffes de peau. Anne Meyer explique que « l'oxygène généré aiderait à relancer la cicatrisation de la zone endommagée, ou pourrait être capable de réaliser une cicatrisation"activée par la lumière" des plaies ».
Ce matériau pourrait révolutionner le secteur du textile. De la mode. Les vêtements créés seraient biodégradables et évolutifs. Un pantalon troué se régénererait, mais un pantalon trop petit pourrait aussi grandir. Si ce n'est qu'hypothétique à l'heure actuelle, cela enlèverait une sacrée épine dans le pied de cette industrie -- l'une des plus polluantes de la Planète. Ces matériaux « peuvent se maintenir sur des périodes de plusieurs semaines et être multipliés sur place, de sorte qu'ils ont le potentiel d'être vraiment durables et partagés partout dans le monde, aussi facilement que le levain », se prend à rêver Anne Meyer.
Ces scientifiques ont enfermé des microalgues dans un produit excrété par des bactéries, vulgairement nommé « cellulose bactérienne ». Les microalgues confèrent des capacités photosynthétiques à l'étoffe obtenue. Ce qui lui permet, notamment, de se régénérer. Les auteurs de l'étude précisent qu'elle peut « survivre de manière stable pendant au moins trois jours sans nutriments », sa durée de vie pouvant être prolongée si elle est transférée vers une nouvelle source de nutriments durant cette période.
Un levain textile
Pour la première fois, ce matériau photosynthétique semble assez performant pour être déployé dans « des applications du monde réel », avance Anne Meyer, biologiste américaine et coautrice du papier. Résistant. Tenace. Flexible. Robuste. Il a tout pour plaire. Déformé d'une façon ou d'une autre, il conserve son intégrité physique. Les chercheurs lui attribuent trois applications principales : la création de feuilles artificielles, de vêtements biologiques, et de peaux photosynthétiques.
Les feuilles artificielles imitent la photosynthèse des feuilles végétales, c'est-à-dire qu'elles convertissent l'eau et le CO2 en oxygène et en énergie, grâce à la lumière du soleil. Cette innovation fait partie des solutions envisagées pour produire de l'énergie et de l'oxygène dans des endroits peu propices à la végétation... comme Mars. En parallèle, les « peaux synthétiques » serviraient pour les greffes de peau. Anne Meyer explique que « l'oxygène généré aiderait à relancer la cicatrisation de la zone endommagée, ou pourrait être capable de réaliser une cicatrisation"activée par la lumière" des plaies ».
Ce matériau pourrait révolutionner le secteur du textile. De la mode. Les vêtements créés seraient biodégradables et évolutifs. Un pantalon troué se régénererait, mais un pantalon trop petit pourrait aussi grandir. Si ce n'est qu'hypothétique à l'heure actuelle, cela enlèverait une sacrée épine dans le pied de cette industrie -- l'une des plus polluantes de la Planète. Ces matériaux « peuvent se maintenir sur des périodes de plusieurs semaines et être multipliés sur place, de sorte qu'ils ont le potentiel d'être vraiment durables et partagés partout dans le monde, aussi facilement que le levain », se prend à rêver Anne Meyer.

 source: lci.fr
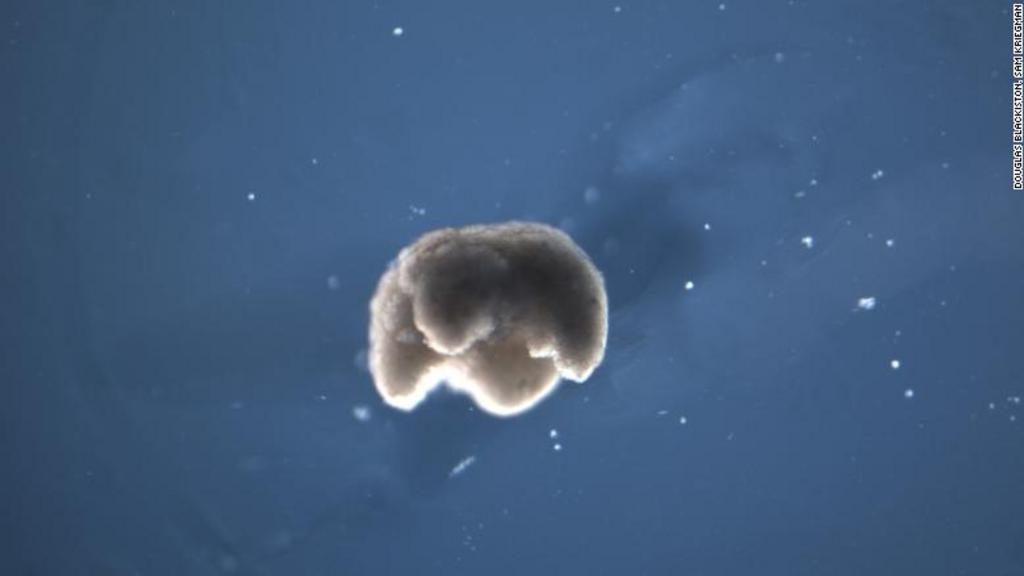
source: lci.frBaptisé "xenobot", ce minuscule organisme a été conçu artificiellement via un programme informatique, dans un laboratoire aux Etats-Unis. A en croire les scientifiques, il pourrait notamment servir à transporter des médicaments en voyageant à l'intérieur du corps humain.
Les robots seront-ils conçus à l'avenir à partir d'animaux ? Moitié machine, moitié organisme vivant, cette drôle de bestiole est un "exobot". Un quoi ? Un exobot. Autrement dit, le premier robot conçu biologiquement par ordinateur à partir de cellules vivantes, dans un laboratoire aux Etats-Unis. Son nom, cette créature, mesurant moins d'un millimètre, le doit à une grenouille africaine à griffes, la Xenopus laevis, dont sont issues les cellules souches ayant servi à façonner cette "machine vivante".
"Ce sont de nouvelles formes de vie", résume Joshua Bongard, informaticien expert en robotique à l'Université du Vermont et co-auteur de l'étude, dans un communiqué de presse. "Ce n'est ni un robot conventionnel ni une espèce animale connue", poursuit le scientifique. Il s'agit d'une nouvelle classe d'artefact : un organisme à la fois vivant et programmable." Pour l'instant, il sait marcher et nager, déplacer des objets. Il peut, en outre, travailler en équipe.
i leur durée de vie peut atteindre plusieurs semaines, les xenobots sont incapables de se reproduire. En revanche, ils sont en mesure de se régénérer. Ils possèdent en effet la capacité de pouvoir survivre sans nutriments supplémentaires pendant des jours, voire des semaines. Cela les rend particulièrement adaptés pour l'administration de médicaments, soulignent les chercheurs des université du Vermont et de Tufts, dont les travaux ont été publiés lundi 13 janvier dans la revue l'Académie nationale américaine des sciences (PNAS).
Plus concrètement, ces robots vivants pourraient servir pour détecter des matériaux radioactifs, récupérer les microplastiques présents dans les océans ou encore encore voyager à l'intérieur du corps humain pour nettoyer les artères, par exemple. Au cours des tests en laboratoire, certains xenobots possédaient d'ailleurs un trou au centre, de quoi leur permettre de transporter des molécules et les administrer localement sans avoir besoin de recourir à une intervention chirurgicale, souligne l'équipe de scientifiques.
Pour façonner ces machines vivantes, les scientifiques ont utilisé le superordinateur Deep Green de l'Université du Vermont. Comme l'explique L'Express, "les scientifiques ont utilisé un algorithme dit évolutionniste - inspiré de la théorie de l'évolution - qui permet de simuler des milliers de modèles candidats à une nouvelle forme de vie, avec pour contrainte de respecter les règles biophysiques d'une cellule de grenouille. Pendant des mois, ce programme informatique a assemblé numériquement des centaines de cellules de grenouilles pour créer une multitude de corps formés différemment."
L'objectif, pour cette partie de l'expérience, était de modéliser l'organisme le plus efficace pour réaliser une tâche bien déterminée. Après plus d'une centaine de tentatives, les modèles les plus aboutis ont été envoyés à des biologistes de l'université de Tufts, dans le Massachusetts. Ces derniers ont utilisé des cellules souches de grenouilles, puis un micro-chirurgien les a façonnées en se servant de pinces microscopiques et d'électrodes afin d'obtenir la forme que le programme informatique dopé à l'intelligence artificielle avait estimé être la meilleure.
https://www.franceculture.fr/emissions/la-methode-scientifique/la-methode-scientifique-emission-du-mercredi-28-avril-2021
Les robots seront-ils conçus à l'avenir à partir d'animaux ? Moitié machine, moitié organisme vivant, cette drôle de bestiole est un "exobot". Un quoi ? Un exobot. Autrement dit, le premier robot conçu biologiquement par ordinateur à partir de cellules vivantes, dans un laboratoire aux Etats-Unis. Son nom, cette créature, mesurant moins d'un millimètre, le doit à une grenouille africaine à griffes, la Xenopus laevis, dont sont issues les cellules souches ayant servi à façonner cette "machine vivante".
"Ce sont de nouvelles formes de vie", résume Joshua Bongard, informaticien expert en robotique à l'Université du Vermont et co-auteur de l'étude, dans un communiqué de presse. "Ce n'est ni un robot conventionnel ni une espèce animale connue", poursuit le scientifique. Il s'agit d'une nouvelle classe d'artefact : un organisme à la fois vivant et programmable." Pour l'instant, il sait marcher et nager, déplacer des objets. Il peut, en outre, travailler en équipe.
i leur durée de vie peut atteindre plusieurs semaines, les xenobots sont incapables de se reproduire. En revanche, ils sont en mesure de se régénérer. Ils possèdent en effet la capacité de pouvoir survivre sans nutriments supplémentaires pendant des jours, voire des semaines. Cela les rend particulièrement adaptés pour l'administration de médicaments, soulignent les chercheurs des université du Vermont et de Tufts, dont les travaux ont été publiés lundi 13 janvier dans la revue l'Académie nationale américaine des sciences (PNAS).
Plus concrètement, ces robots vivants pourraient servir pour détecter des matériaux radioactifs, récupérer les microplastiques présents dans les océans ou encore encore voyager à l'intérieur du corps humain pour nettoyer les artères, par exemple. Au cours des tests en laboratoire, certains xenobots possédaient d'ailleurs un trou au centre, de quoi leur permettre de transporter des molécules et les administrer localement sans avoir besoin de recourir à une intervention chirurgicale, souligne l'équipe de scientifiques.
Pour façonner ces machines vivantes, les scientifiques ont utilisé le superordinateur Deep Green de l'Université du Vermont. Comme l'explique L'Express, "les scientifiques ont utilisé un algorithme dit évolutionniste - inspiré de la théorie de l'évolution - qui permet de simuler des milliers de modèles candidats à une nouvelle forme de vie, avec pour contrainte de respecter les règles biophysiques d'une cellule de grenouille. Pendant des mois, ce programme informatique a assemblé numériquement des centaines de cellules de grenouilles pour créer une multitude de corps formés différemment."
L'objectif, pour cette partie de l'expérience, était de modéliser l'organisme le plus efficace pour réaliser une tâche bien déterminée. Après plus d'une centaine de tentatives, les modèles les plus aboutis ont été envoyés à des biologistes de l'université de Tufts, dans le Massachusetts. Ces derniers ont utilisé des cellules souches de grenouilles, puis un micro-chirurgien les a façonnées en se servant de pinces microscopiques et d'électrodes afin d'obtenir la forme que le programme informatique dopé à l'intelligence artificielle avait estimé être la meilleure.
https://www.franceculture.fr/emissions/la-methode-scientifique/la-methode-scientifique-emission-du-mercredi-28-avril-2021




 16.09.2023 - 06h34
16.09.2023 - 06h34